Устройства методи за производство на сярна киселина. Свържете се с производството на сярна киселина
Получаването на сярна киселина по контактния метод включва четири етапа: производство на серен диоксид; пречистване на газ от примеси, получаване на серен триоксид; абсорбция на серен триоксид.
Първият етап включва производството на диоксид от пирити, които се изгарят в пещи, където протича необратима реакция. Газът за изгаряне след почистване на прах в електростатични утаители има температура около 350 ° C и съдържа остатъци от прах, както и газообразни примеси от арсенови съединения (As2O3), селен (SeO2) и други елементи, които могат да унищожат катализатора и да намалят неговата активност. Препоръчително е да се добиват примеси от селен от газ и като материал, необходим за промишлеността. За пречистване на газ е предвидена система от миещи кули, електростатични утаители и сушилни кули. Третият етап на производството на сярна киселина е основният. Сухият пречистен газ навлиза в контактното окисление на SO2 до SO3, което се получава чрез обратима екзотермична реакция, която протича с намаляване на обема на газа:
Скоростта на окисляване на SO2 в отсъствие на катализатор е дори ниска при високи температури.
Заводите със сярна киселина у нас използват главно ванадийни контактни маси със съдържание на V2Os около 7%, както и оксиди на алкални метали и силно порести алумосиликати като носители.
В четвъртия етап на процеса на производство на сярна киселина охладеният окислен газ се изпраща в отдела за абсорбция (абсорбция) на цеха. Не е препоръчително да се абсорбира триоксидът с вода, тъй като реакцията на SOs + FbO- ^ HaSO ^ Q ще протече в газовата фаза (поради освободената топлина водата се превръща в пара) с образуването на дребни капчици киселина (мъгла), което е много трудно да се улови. Следователно, SO3 се абсорбира в концентрирана сярна киселина на два етапа.
50. Области на приложение на сярна киселина и технически и икономически показатели за нейното производство.
Производството на сярна киселина - една от най-силните и най-евтините киселини - е от голямо икономическо значение, поради широкото й използване в различни индустрии.
Безводната сярна киселина (монохидрат) е тежка мазна течност (плътност при 20 ° C 1830 kg / m3, точка на кипене 296.2 ° C при атмосферно налягане; температура на кристализация 10.45 ° C). Смесва се с вода във всяко съотношение със значително отделяне на топлина (образуват се хидрати). Серен оксид се разтваря в сярна киселина. Такова решение, чийто състав се характеризира със съдържанието на свободен SO3, се нарича олеум.
Сярна киселина се използва за производството на торове - суперфосфат, амофос, амониев сулфат и др. Потреблението му е значително за рафиниране на нефтопродукти, както и за цветна металургия, и за офорт на метали. Високочистата сярна киселина се използва при производството на багрила, лакове, бои, лекарства, някои пластмаси, химически влакна, много пестициди, експлозиви, етери, алкохоли и др.
Сярна киселина се произвежда по два начина: контактна и азотна (кула). Около 90% от общото производство на киселина се получава по контактния метод, тъй като това осигурява висока концентрация и чистота на продукта.
Като суровини за производството на сярна киселина елементарна сяра и серен пирит; Освен това широко се използват промишлени отпадъци, съдържащи сяра.
Серният пирит се характеризира със съдържание на сяра 35 ... 50%. Сулфидните руди, които се използват при производството на цветни метали (Cu, Zn, Pb и др.), Често присъстват в находища на серен пирит.
Сулфидните руди се калцинират, по време на които се образуват газове от серен диоксид, които се използват за производството на сярна киселина. Понастоящем сероводородните газове, генерирани по време на рафинирането на нефт, коксуването на въглища, както и получените при рафиниране на природен газ, служат като суровина за неговото производство.
Най-просто е производството на сярна киселина от сяра, извлечена от местни руди или от странични продукти на редица отрасли (газова сяра). Въпреки това, цената на киселина, получена от сяра, е по-висока, отколкото от пиритите. Освен това сярата е необходима за производството на каучук, кибрит, въглероден дисулфид, пестициди, лекарства и др.
На настоящия етап се осигурява снабдяването на промишлеността със серосъдържащи суровини чрез разработване на естествена и производство на свързана сяра. В черната и черната металургия, газовата и нефтохимическата промишленост сярата се получава от газови кондензати. Следователно, производството на флотационни пирити в предприятията за цветна металургия се увеличава.
Разработва се технология за преработка на нови видове суровини: сулфатно печене на колективен сулфиден концентрат на Соколовско-Сарбайския комплекс и изпичане на нестандартни пирити.
Процесът на получаване на сярна киселина по контактния метод е значително опростен, ако сярата, която е почти без арсен, или сероводород, получен от пречистването на горими газове и нефтопродукти, се използват като суровина за получаване на СО. Когато се използва разтопената сяра като суровина, процесът на производство на сярна киселина включва три етапа: изгаряне на сяра в дюзови пещи; окисляване на серен диоксид до триоксид в контактни устройства; абсорбция на серен триоксид.
Промишлеността произвежда техническа, акумулаторна и реактивна сярна киселина. Тези видове киселини се различават по предназначение и съдържание на основния компонент и примеси.
Перспектива по отношение на подобряването на техническите и икономическите показатели за производството на сярна киселина са системите за почистване на сух газ. Класическият контактен метод за неговото производство включва редица противоположни процеси: горещият калциниращ газ се охлажда в отделението за обработка, след което отново се нагрява в контакта; в кулите за миене газът се навлажнява, в сушилните кули се изцежда старателно. В СССР на базата на научни изследвания е създаден нов процес за производство на сярна киселина - химическо чистене (СО). Основната характеристика на процеса на СО е, че след напушване горещият калциниращ газ без охлаждане, измиване и сушене се изпраща директно към контактния апарат. Това се осигурява от такъв режим на работа на пещи с суспендиран (кипящ) слой пирит, при който значителна част от съединенията на арсена се адсорбират от шлака. По този начин, вместо четирите етапа на класическия процес, СО включва само три, поради които капиталовите инвестиции се намаляват с 15 ... 25%, разходите за сярна киселина - с 10 ... 15%.
Предвижда се увеличаване на капацитета на съществуващите и в строителството предприятия за производство на сярна киселина по контактен метод с малки допълнителни разходи. Това ще бъде постигнато чрез увеличаване на концентрацията на SO2 в преработените газове, както и чрез въвеждане на кратка схема при преминаване от изпичане на пирит към горене на сяра. За да се подобри хардуерната конструкция на процеса, беше разработен контактен апарат с успоредни слоеве катализатор (неговата консумация на метал стана 25% по-ниска). Използването на хладилници с черупки и тръби с анодна защита ще удължи техния експлоатационен живот до 10 години.
Технологията за производство на сярна киселина по азотен метод се актуализира чрез подобряване на куловите системи. Изчисленията показват, че в сравнение с контактния метод за преработка на газове, получени по време на изпичането на пирит във въздуха, с азотен метод и инсталиране на същия капацитет (180 хиляди тона годишно), капиталовите разходи се намаляват с 43,6%, разходите за преработка на серен диоксид - с 45 , 5, намалени разходи - с 44,7, а интензивността на труда - с 20,2%.
Големите потребители на сярна киселина трябва да я произвеждат в своите предприятия, независимо от ведомствената принадлежност, това ще намали натоварването на железопътния транспорт и необходимостта от резервоари 3 пъти.
Използването на отработени сярни киселини при производството на минерални торове ще се увеличи след тяхното пречистване и регенерация.
МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО НА РЕПУБЛИКА БЕЛАРУС
БЪЛГАРСКИ ДЪРЖАВЕН ИКОНОМИЧЕСКИ УНИВЕРСИТЕТ
Катедра по технологии
Индивидуална работа по темата:
"Производство на сярна киселина по контактен метод."
Изпълнен от студент от I курс на FWA: Клименок М.А.
Проверен от учителя: Тарасевич В.А.
Минск 2002
· Резюме
· Описание на контактния метод за производство на сярна киселина
· Основната технологична схема на производството на сярна киселина по контактен метод
· Динамика на разходите за труд в развитието на технологичния процес
· Изчисляване на нивото на технологиите, оръжията и производителността на живия труд
· Заключение
· Литература и източници
Тази работа се състои от 12 страници.
Ключови думи: сярна киселина, Метод за контакт, Реакция, Технология на производство, Динамика на разходите за труд, Технологичен процес.
В тази работа беше проучена и описана технологията за контактна сяра. Дадени са илюстрации, диаграми, графики и таблици, отразяващи същността на процеса. Определени са най-важните тенденции в развитието на производството на сярна киселина по контактния метод
Анализът на динамиката на разходите за труд на живия и миналия труд, както и на динамиката на разходите за труд в развитието на технологичния процес. Изчислява се нивото на технологията, въоръжението и производителността на живия труд. Изводите и изводите се правят.
Описание на контактния метод за производство на сярна киселина
Контактният метод произвежда голям брой разновидности на сярна киселина, включително олеум, съдържащ 20% свободен SO3, витриолово масло (92,5% H 2 SO 4 и 7,5% H 2 O), акумулаторна киселина, приблизително в същата концентрация като и масло от витриол, но по-чисто.
Контактният метод за производство на сярна киселина включва три етапа: пречистване на газ от вредни за катализатора примеси; контактно окисление на серен диоксид до сяра; абсорбция на серен анхидрид от сярна киселина. Основният етап е контактното окисление на SO2 до SO 3; името на тази операция се отнася до целия метод.
Контактното окисляване на серен диоксид е типичен пример за хетерогенна окислителна екзотермична катализа. Това е една от най-изследваните каталитични синтези.
Обратимо реакционно равновесие
2SO 2 + O2\u003e< 2 SO 3 + 2 x 96,7 кдж (500 оС) (а)
в съответствие с принципа на Le Chatelier, той се измества към образуването на SO 3 с намаляваща температура и увеличаващо се налягане; съответно степента на равновесна конверсия на SO2 в SO 3 се увеличава
Трябва да се отбележи, че увеличаването на налягането естествено увеличава скоростта на реакция (a). Въпреки това е нерационално да се използва повишено налягане в този процес, тъй като освен реакция на газовете, баластният азот ще трябва да се пресова, което обикновено съставлява 80% от цялата смес и следователно катализаторите се използват активно в производствения цикъл.
Най-активният катализатор е платината, но тя излезе от употреба поради високата цена и лесното отравяне от примеси на изгарящ газ, особено арсен. Железният оксид е евтин, но с обичайния газов състав от 7% SO2 и 11% O2, той проявява каталитична активност само при температури над 625 ° C, т.е. когато XP 70% и следователно се използва само за първоначалното окисляване на SO2 за постигане на XP 50-60%. Ванадиевият катализатор е по-малко активен от платиновия, но по-евтин и отровен от арсенови съединения няколко хиляди пъти по-малко от платинен; той се оказа най-рационален и само той се използва при производството на сярна киселина. Ванадийната контактна маса съдържа средно 7% V2O5; активаторите са алкални метални оксиди; обикновено се използва активатор на K2O; носителят е порест алумосиликат. Понастоящем катализаторът се използва под формата на съединения SiO2, K  и / или Cs, V в различни пропорции. Такова съединение се оказа най-устойчивото на киселина и най-стабилното. В цял свят по-правилното му име е „съдържащ ванадий“. Такъв катализатор е специално проектиран да работи с ниски температури, което води до по-ниски емисии. В допълнение, такава катализа е по-евтина от калий / ванадий. Общите ванадийни контактни маси са порести гранули, таблетки или пръстени (фиг. 1).
и / или Cs, V в различни пропорции. Такова съединение се оказа най-устойчивото на киселина и най-стабилното. В цял свят по-правилното му име е „съдържащ ванадий“. Такъв катализатор е специално проектиран да работи с ниски температури, което води до по-ниски емисии. В допълнение, такава катализа е по-евтина от калий / ванадий. Общите ванадийни контактни маси са порести гранули, таблетки или пръстени (фиг. 1).
При условия на катализа калиев оксид се превръща в K2S2O7, а контактната маса обикновено е порест носител, чиято повърхност и пори се навлажняват с филм от разтвор на ванадиев пентоксид в течен калиев пиросулфат.
Ванадиевата контактна маса работи при температури от 400 до 600 ° C. С повишаване на температурата над 600 ° C започва необратимо намаляване на активността на катализатора поради синтероването на компоненти с образуването на неактивни съединения, неразтворими в калиев пиросулфат. С понижаване на температурата активността на катализатора рязко намалява поради превръщането на пентавалентния ванадий в тетравалент с образуването на неактивен ванадил VOSO4.
Процесът на катализа се състои от етапите: 1) дифузия на реагиращите компоненти от ядрата на газовия поток към гранулите и след това в порите на контактната маса; 2) сорбция на кислород от катализатора (пренос на електрон от катализатора към кислородните атоми); 3) сорбция на SO2 молекули с образуването на катализаторния комплекс SO2 * O *; 4) пренареждане на електрони с образуването на каталитичен комплекс SO2 *; 5) десорбция на SO3 от порите на контактната маса и от повърхността на зърната.
При големи гранули от контактна маса общата скорост на процеса се определя от дифузията на реагентите (1-ви и 6-ти етап). Обикновено получават гранули с диаметър не повече от 5 mm; процесът протича на първите етапи на окисление в дифузията, а в последния (при х 80%) в кинетичната област.
Поради унищожаването и залепването на гранули, замърсяването на слоя, отравянето на катализатора от арсенови съединения и температурното му увреждане при случайни нарушения на режима, контактната маса с ванадий се подменя средно след 4 години. Ако газовото пречистване, получено чрез изпичане на пирити, е нарушено, тогава работата на контактния апарат е нарушена поради отравяне на първия слой от контактната маса след няколко дни. За да се запази активността на катализатора, се използва пречистване на тънки газове по мокър метод.
Принципна схема на производството на сярна киселина по контактен метод
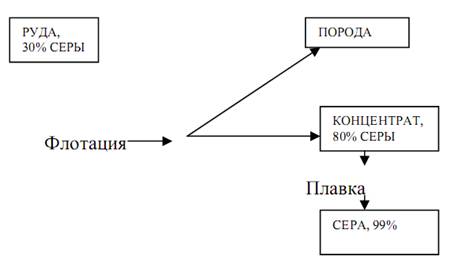
Най-добрите суровини за производство кисел газ служи като сяра, която се топи от естествени скали, съдържащи сяра, и също се получава като страничен продукт при производството на мед, при пречистването на газове и др. Сярата се топи при температура от 113 градуса С, тя е лесно запалима и гори в прости пещи (фиг. 2). Оказва се газ с висока концентрация, с малко съдържание на вредни примеси.
Сярата се изгаря от реакцията S + O 2\u003e SO 2 + 296 kJ. Всъщност сярата се стопява и се изпарява преди изгаряне (т.е. bp ~ 444 ° C) и изгаря в газовата фаза. По този начин самият процес на горене е хомогенен.

Компресор и горивна камера
Неизгоряла сяра
Въздух за горене и горене
Течна сяра
Сгъстен въздух
Продукт - Газов газ

схема на производство на сярна киселина
1 - 1-ва кула за измиване; 2 - 2-ра измивна кула с накрайник; 3 - мокър електростатичен утаител; 4 - сушилна кула с накрайник; 5 - турбокомпресор; 6 - тръбен топлообменник; 7 - контактно устройство; 8 - тръбен газов хладилник; 9 и 10 - абсорбционни кули с накрайник; 11 - центробежни помпи; 12 - киселинни колекции; 13 - киселинни хладилници
След грубо почистване на прах от утайки с електростатични утайки при температура около 300 ° С, калциниращият газ влиза в кулата за измиване (Фиг. 3: 1,2), където се разпръсква студена сярна киселина (75% Н 2 SO 4). Когато газът се охлади, съдържащият се в него серен анхидрид и водната пара се кондензират под формата на малки капчици. Арсеновият оксид се разтваря в тези капчици. Образува се мъгла от арсенова киселина, която частично се улавя в първата кула, а във втората кула с керамична дюза. В същото време се улавят следи от прах, селен и други примеси. Образува се мръсна сярна киселина (до 8% от общата продукция), която се дава като нестандартни продукти. Окончателното пречистване на газа от неуловимата арсеново-кисела мъгла се извършва във влажни филтри (фиг. 3: 3), които се инсталират последователно (две или три). Принципът на работа на мокрите филтри е същият като на сухите. Капки мъгла се отлагат върху тръбни електроди за валежи, направени от олово или „ATM“ пластмаса, и текат надолу. Пречистването на газа завършва чрез изсушаването му от водна пара със сулфатно масло в кула с накрайник (фиг. 3: 4). Обикновено са монтирани две сушилни кули. Кулите, каналите и колекторите за киселини в отдела за почистване обикновено инсталират стомана, облицована с устойчива на киселина тухла или диабаза. Сухият серен диоксид и серният анхидрид не са агресивни, следователно цялото последващо оборудване до монохидратния абсорбатор може да бъде монтирано от обикновена въглеродна стомана без защита от корозия.
Голям брой оборудване създава значителна устойчивост на газовия поток (до 2 м воден стълб), поради което е инсталиран турбокомпресор за транспортиране на газ (фиг. 3: 5). Компресорът, изсмукващ газ от пещите през цялото оборудване, го изпомпва в контактния възел.
Контактният възел (фиг. 3: 6,7,8) се състои от контактен апарат, топлообменник с обвивка и тръба и не е показан на диаграмата (фиг. 4). газов нагревател. В топлообменника на стартовия нагревател газът се загрява преди да влезе в устройството по време на стартиране или когато температурата в устройството падне под нормалната.
Обикновено използвани устройства за контакт на рафтове. Такова устройство има цилиндрично тяло с диаметър от 3 до 10 и височина 10-20 м. Вътре в тялото са инсталирани четири до пет решетки със слой гранули от контактна маса върху всяка от тях. Между слоевете контактна маса са монтирани междинни тръбни или кутийкови топлообменници. Диаграмата показва четирислоен контактен апарат, въпреки че по-често се използват петслойни апарати, но принципът на тяхното действие е напълно подобен, разликата е само в още един слой на катализатора. Пресният газ се нагрява от топлината на реагирания горещ газ, първо във външния топлообменник, след това той частично или напълно преминава за загряване на три до четири вътрешни топлообменници последователно, при 440-450 ° С влиза в първия слой от контактната маса. Тази температура се контролира чрез отваряне на клапаните на затворите. Основната цел на вътрешните топлообменници е да охлаждат частично окисления и нагрят газ в слоя на катализатора, така че режимът стъпаловидно да се приближава до кривата на оптимални температури.
 Устройства за контакт с рафтове - един от най-често срещаните видове устройства за контакт. Принципът на тяхното действие е, че нагряването и охлаждането на газ между слоевете на катализатора, разположени на рафтовете, се осъществяват в самия контактен апарат, като се използват различни охлаждащи течности или методи за охлаждане. например гости-. се увеличава по протежение на газа и височината на топлообменниците намалява, тъй като с увеличаване на общата степен на преобразуване скоростта на реакцията намалява и съответно количеството отделена топлина намалява. Пресният газ тече последователно отдолу нагоре в пръстеновидното пространство на топлообменниците, охлаждайки продуктите от реакцията и загрявайки до температурата на началото на реакцията
Устройства за контакт с рафтове - един от най-често срещаните видове устройства за контакт. Принципът на тяхното действие е, че нагряването и охлаждането на газ между слоевете на катализатора, разположени на рафтовете, се осъществяват в самия контактен апарат, като се използват различни охлаждащи течности или методи за охлаждане. например гости-. се увеличава по протежение на газа и височината на топлообменниците намалява, тъй като с увеличаване на общата степен на преобразуване скоростта на реакцията намалява и съответно количеството отделена топлина намалява. Пресният газ тече последователно отдолу нагоре в пръстеновидното пространство на топлообменниците, охлаждайки продуктите от реакцията и загрявайки до температурата на началото на реакцията
Производителността на контактните устройства по отношение на H 2 SO 4, в зависимост от техния размер, варира от 50 до 500 тона на H 2 SO 4 на ден. Проектирани контактни устройства с капацитет 1000 и 2000 тона на ден. 200-300 литра контактна маса на 1 тон дневна продукция се зареждат в апарата. Тръбните контактни устройства се използват за окисляване на SO 2 по-рядко от тези на рафт. За окисляване на серния газ с повишена концентрация е рационално да се използват контактни устройства с кипящ каталитичен слой.
Абсорбцията на серен анхидрид чрез реакцията SO 3 + H 2 O \u003d H 2 SO 4 +9200 J обикновено се извършва в кули с накрайник (фиг. 3: 9,10), тъй като спаринг или пяна абсорбатори с големи натоварвания имат повишена хидравлична устойчивост. Ако парциалното налягане на водната пара върху абсорбиращата киселина е значително, тогава SO 3 се комбинира с Н20 в газовата фаза и образува най-малките капчици неуловима сярна киселина. Следователно абсорбцията е концентрирани киселини, Най-добрият абсорбиращ капацитет е киселина, съдържаща 98,3% H2S04 и притежаваща пренебрежима еластичност както на водна пара, така и на SO3. За един цикъл в кулата обаче е невъзможно да се фиксира киселина от 98,3% до стандартен олеум, съдържащ 18,5-20% свободен серен анхидрид. Поради големия термичен ефект на абсорбция по време на адиабатния процес в кулата, киселината се загрява и абсорбцията спира. Следователно, за да се получи олеум, абсорбцията се извършва в две последователно инсталирани кули с накрайник: първата от тях се напоява с олеум, а втората - с 98,3% сярна киселина. За да се подобри абсорбцията, газът и киселината, постъпващи в абсорбера, се охлаждат, докато движещата сила на процеса се увеличава.
Във всички кули контактно производство, включително абсорбатори, количеството напоителна киселина е многократно по-голямо от необходимото за усвояването на газовите компоненти (H 2 O, SO 3) и се определя от топлинния баланс. За охлаждане на циркулиращите киселини обикновено се инсталират напоителни хладилници, в тръбите на които, напоени със студена вода отвън, тече охладената киселина.
Производството на сярна киселина е значително опростено чрез обработка на газ, получен чрез изгаряне на предварително разтопена и филтрирана естествена сяра, която е почти без арсен. В този случай чистата сяра се изгаря на въздух, който преди това се изсушава със сярна киселина в кула с накрайник. Оказва се газ с 9% SO2 и 12% O2 при температура 1000 ° C, който първо се изпраща под парен котел, а след това без почистване в контактно устройство. Интензитетът на апарата е по-голям, отколкото на пиритовия газ, поради повишената концентрация на SO2 и O2. В апарата няма топлообменници, тъй като температурата на газовете се намалява чрез добавяне на студен въздух между слоевете. Абсорбцията на SO3 се осъществява по същия начин, както в технологичната схема.
Най-важните тенденции в развитието на производството на сярна киселина по контактен метод:
1) интензифицирането на процесите чрез провеждането им в суспендиран слой, използването на кислород, производството и преработката на концентриран газ, използването на активни катализатори;
2) опростяване на методите за почистване на газ от прах и контактни отрови (по-кратка схема на потока);
3) увеличаване на мощността на оборудването;
4) цялостна автоматизация на производството;
5) намаляване на съотношението на разходите за суровини и използването на серосъдържащи отпадъци от различни отрасли като суровини;
6) неутрализиране на отработените газове.
Динамиката на разходите за труд в развитието на технологичния процес
Като цяло, всички горепосочени материали могат да бъдат представени, както следва:

Известно е, че този процес и динамиката на труда се характеризират със следните формули:
Tl \u003d ---------------------- Tn \u003d 0,004 * t 2 +0,3 Tc \u003d Tl + Tn
Връзката между тези формули е следната:
Tp \u003d 0,004 * - 75 +0,3 и Tzh \u003d 21 * Tp-0,3 +1575
Въз основа на горните формули ще извършим изчисленията и ще ги внесем в обща таблица (Таблица 1):
| (Табл. 1): Динамика на разходите за труд при производството на сярна киселина за 15 години |
|||||||||||||||
| t (Време, години) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Разходи за жизнения труд | 0,78 | 0,75 | 0,71 | 0,654 | 0,595 | 0,54 | 0,48 | 0,43 | 0,38 | 0,34 | 0,3 | 0,27 | 0,24 | 0,22 | 0,198 |
| Минали разходи за труд | 0,3 | 0,32 | 0,34 | 0,364 | 0,4 | 0,44 | 0,496 | 0,56 | 0,62 | 0,7 | 0,78 | 0,88 | 0,98 | 1,08 | 1,2 |
| Общи разходи | 1,09 | 1,07 | 1,04 | 1,018 | 0,995 | 0,98 | 0,976 | 0,98 | 1,01 | 1,04 | 1,09 | 1,15 | 1,22 | 1,3 | 1,398 |
Въз основа на таблицата изграждаме графики на зависимостите на Tl, Tn, Tc от времето (фиг. 7) и зависимостите на Tj от Tn (фиг. 6) и Tn от Tl (фиг. 8).

От тази графика се вижда, че този процес е ограничен в своето развитие.
Икономическата граница на натрупването на предишен труд ще настъпи след седем години.


Графики 7 и 8 показват, че типът процес е икономия на труд.
Изчисляване на нивото на технологиите, оръжията и производителността на живия труд.
Нивото на технологията се изчислява по формулата:
Комфорт \u003d 1 / TJ * 1 / TP
Производителност на труда на живо:
L \u003d за тези * B
Техническото оборудване се изчислява:
B \u003d TP / TJ
Относително ниво на технология:
Watnos \u003d Комфорт / L
Ще извършим изчисления, използвайки горните формули и ще въведем данните в таблицата (Таблица 2):
| T Време (години) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| Разходи за жизнения труд | 0,78 | 0,75 | 0,71 | 0,654 | 0,595 | 0,54 | 0,48 | 0,43 | 0,38 | 0,34 | 0,3 | 0,27 | 0,24 |
| Минали разходи за труд | 0,3 | 0,32 | 0,34 | 0,364 | 0,4 | 0,44 | 0,496 | 0,56 | 0,62 | 0,7 | 0,78 | 0,88 | 0,98 |
| Общи разходи | 1,09 | 1,07 | 1,04 | 1,018 | 0,995 | 0,98 | 0,976 | 0,98 | 1,01 | 1,04 | 1,09 | 1,15 | 1,22 |
| Технологично ниво | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 | 4,2 |
| Tech. въоръжаване | 0,39 | 0,42 | 0,47 | 0,556 | 0,672 | 0,83 | 1,033 | 1,3 | 1,64 | 2,058 | 2,58 | 3,22 | 4 |
| Изпълнение TJ | 1,28 | 1,33 | 1,41 | 1,529 | 1,68 | 1,86 | 2,083 | 2,34 | 2,62 | 2,94 | 3,29 | 3,68 | 4,1 |
| Ниво на технологията за връзка | 3,29 | 3,16 | 2,98 | 2,747 | 2,5 | 2,25 | 2,016 | 1,8 | 1,6 | 1,429 | 1,28 | 1,14 | 1,02 |
От тази таблица се вижда, че рационалното развитие е препоръчително само за седем години, тъй като в този период на време относителното ниво на технологиите е по-голямо от производителността на живия труд.
заключение
В тази статия се изследва и описва технологията за контактна сяра, анализирана е динамиката на разходите за труд на живия и миналия труд, както и динамиката на разходите за труд по време на развитието на технологичния процес. Въз основа на извършената работа бяха получени следните изводи: Развитието на тези процеси е ограничено, икономическата граница на натрупването на миналия труд е седем години, този технологичен процес е икономия на труд и рационалното развитие е целесъобразно за седем години.
Литература и източници:
1. ПРОИЗВОДСТВО НА Сярна киселина / Бараненко Д. http://service.sch239.spb.ru:8101/infoteka/root/chemistry/room1/baran/chem.htm
2. Технология на най-важните отрасли: Учебник. За екв. Spec. Университети / A.M. Ginberg, B.A. Khokhlov. - М.: Висше училище, 1985г.




Етапи - приготвяне на суровини и неговото изгаряне или изпичане. Съдържанието и хардуерният им дизайн значително зависят от естеството на суровината, което до голяма степен определя сложността на технологичното производство на сярна киселина. 1. Железен пирит. Естественият железен пирит е сложна скала, състояща се от железен сулфид ReB2, сулфиди на други метали (мед, цинк, олово и др.), ...


Не винаги е възможно. В същото време отработените газове са най-евтините суровини, цените на едро за пиритите също са ниски, докато сярата е най-скъпата суровина. Следователно, за да може производството на сярна киселина от сяра да бъде икономически осъществимо, трябва да се разработи схема, при която разходите за нейната преработка ще бъдат значително по-ниски от разходите за преработка на пирити или отпадъци ...
![]()
За автоматичното регулиране е необходимо да се знаят възможно най-много изискванията на различни химико-технологични процеси. 1. Основната част 1.1 Технологичният процес за получаване на сярен анхидрид при производството на сярна киселина. Контактното производство на сярна киселина се състои от следните действия: 1. Разтоварване, съхранение и приготвяне на суровини ...
Образува се азотна киселина: NO (HSO4) + H2O®H2SO4 + HNO2 Освен това окислява SO2 съгласно уравнението: SO2 + 2HNO2®H2SO4 + 2NO 75% сярна киселина се натрупва в долната част на кули 1 и 2, разбира се, в по-голямо количество отколкото е изразходвано за приготвяне на нитроза (в края на краищата се добавя „новородена“ сярна киселина). Азотният оксид NO се връща отново към окисляване. Тъй като определена сума ...
През 13 век сярна киселина се получава чрез изпичане на меден сулфат. Оттук и древното име на сярна киселина - витриолово масло. От 18-ти век сярната киселина се получава по азотен метод, който се запазва и до днес. В нашия регион получи сярна киселина. У нас има 2 основни метода за производство на сярна киселина: азотна и контактна. Според всеки от методите първият етап е окисляването на съдържащи сяра суровини с атмосферен кислород за получаване на серен оксид (IV). Окислява се до SO3. При азотния метод катализаторите са азотни оксиди в кулите в течна фаза. Концентрацията му е 75%. Съдържа голямо количество примеси. Много е евтин и отива за производството на торове. Екологично производството на кула киселина е много мръсно. Понастоящем новите инсталации вече не се строят, но стари инсталации ще съществуват дълго време поради ниската цена на получената киселина.
Контактният метод използва твърд катализатор за окисляване на SO2 до SO3. В последния етап S03 взаимодейства с вода, за да образува сярна киселина. Този метод е екологичен.
Теоретичната основа за производството на сярна киселина по контактен метод.
Процесът се състои от 4 етапа:
1. Изгаряне на серен пирит.
2. Пречистване на пещния газ от каталитични отрови.
3. Каталитично окисляване на SO2 до SO3.
4. абсорбция на SO3 на 98% сярна киселина или олеум.
Получаване на SO2. Получава се при печене на пирит, който е част от пиритите с въздушен кислород.
4FeS2 + 11O2 --- (600-800С) ---\u003e 2Fe2O3 + 8SO2 + топлина
Това е хетерогенна, високотемпературна реакция, необратима, некаталитична. По време на изпичането на повърхността на пиритовите частици се образува соя от железен оксид, което инхибира реакцията на окисляване. Скоростта на хетерогенна реакция зависи от интерфейса. Необходимо е да се смила пирит. По време на процеса дебелината на оксидния филм непрекъснато се увеличава и предотвратява по-нататъшната реакция на окисляване, процесът преминава в зоната на вътредифузия. За да се премахнат тези дифузионни инхибиции, пиритът трябва да бъде смлян, докато дебелината на оксидния филм автоматично намалява.
При преминаване към микро антитела, микрочастиците на пирита при температура над 900 градуса започват да се сливат с образуването на големи агломерати. Следователно температурата е ограничена до 600-900 градуса.
Процесът на дифузия по повърхността на пирита протича по следния начин: молекулите на кислорода текат вътре в пиритното зърно и реагират с образуването на железен оксид и SO2. Полученият SO2 се десорбира от пиритовите частици, за да образува SO2 облак около частицата, който предотвратява проникването на кислород в пиритната частица. За да се отстрани този недостатък, пиритовите частици трябва енергично да се смесват.
Почистване на газова печка.
Полученият газ от пещта първо се охлажда от по-голямата част от праха в циклона, след охлаждане .....
След охлаждане пещният газ съдържа голямо количество примеси - селен, арсен, железни оксиди, влага и др.
Много примеси са контактни отрови за окисляване на SO2 до SO3. Следователно е необходимо почистване и сушене на пещния газ.
Към днешна дата може ефективно да се извършва само мокро почистване.
Вредните примеси се абсорбират последователно със 70%, 35%, 5% сярна киселина и вода. След това получената сярна киселина се суши, която след това се избира като търговски продукт.
Проблемна ситуация: на етапа на почистване газът от пещта се охлажда, навлажнява, а на следващия етап ще трябва да се нагрее до висока температура и да се изцеди.
Окисляване на SO2 до SO3.
Това е екзотермична каталитична обратима реакция, протичаща с намаляване на обема.
2SO2 + O2 \u003d 2SO3 + Q
Според принципа на Le Chatelier, той трябва да се извършва при ниска температура и високо налягане. В момента този процес се осъществява без прилагане на налягане поради високата концентрация на азотен баласт.
Без катализатор, тази реакция практически не преминава.Прилагат се следните катализатори - платина - той е много активен, но много катализатор, много е отровен от контактни отрови; ванадиев оксид - активен при температура 400-600 градуса, запушванията са ецвани с контактни отрови, е основният катализатор; железният оксид 3 е евтин, не се ецва от контактни отрови, но е активен при температури над 625 градуса, при които равновесната степен на конверсия не може да бъде по-висока от 70%. Използва се за предварително окисляване на SO2 до SO3 с конверсия от 50-60%.
Ефектът на температурата.
По време на процеса на окисляване непрекъснато се генерира топлина, което води до непрекъснато повишаване на температурата в реактора. За да издържи температурата в реактора, реакторът е многостъпален и топлината се отделя след всеки етап.
Равновесна степен на конверсия. За да се измести степента на равновесие надясно и да се постигне обща степен на преобразуване близо до 100%, е разработена система DK / YES - двойно контактуване и двойно поглъщане. След първия етап на контакт (1-3 рафтове на реактора, общо 5) контактният газ се абсорбира, за да се извлече SO3, образуван от него. Равновесната степен на конверсия на този етап е 93%. Останалият SO2 се връща в реактора на 2-ри етап на контакт (4-5 рафтове на реактора), където отново 93% от SO2 се превръща в SO3. И след това преминава към втория етап на усвояване. Общата степен на конверсия е: 99,5%.
Абсорбция на серен оксид VI.
SO3 + H2O -\u003e H2SO4 + Q
Поради възможността от замъгляване ... водата не може да се използва като абсорбиращ; използва се 98% сярна киселина (налягане на парите 0) или 19% олеум.
Тази реакция е разнородна, следователно е необходимо увеличаване на интерфейса между газовата и течната фаза. За целта се използват плочи и много висока плътност на напояване на колоните. Напояването се извършва с 19% олеум, получават се 20% олеум. Тази реакция може да се извърши във фазата на парата с много висока скорост, докато е необходимо да се утаи мъгла от сярна киселина върху електростатичните утаители.
Дизайнът на оборудването е значително опростен.
Абсорбцията е практически необратима при температури над 500 градуса.
Технологичната схема за производство на сярна киселина по контактния метод на DC / ДА.
Получавайте непрекъснат метод на 4 етапа.
1. Окисляване на серни пирити с атмосферен кислород до серен оксид 4.
2. Мокро почистване на серни оксиди 4 от контактни отрови.
3. Контакт на окисление на серен оксид 4 до серен оксид 6 върху хетерогенен ванадиев катализатор.
4. Абсорбция на серен оксид 6 98% сярна киселина и олеум.
В пещното легло 1 пещ, непрекъснато се подава натрошени серни пирити и въздух (излишък 1,5). Полученият газ от пещта се почиства от прах в циклон 2, охлажда се в котел за отработена топлина 3, преминава електростатичен утаител 4 за отстраняване на остатъците от прах и след това преминава към мокро почистване. Мокрото почистване е скъпо, но само днес е в състояние да почисти пещния газ от контактни отрови - оксиди от селен, арсен, водни пари. Мокрото почистване се извършва в миещи кули, мокри електростатични утаители и сушилни кули. За да направите това, пещният газ преминава последователно през измиващи кули 5,6,8, които се напояват със 70% сярна киселина (5), 35% сярна киселина (6), 5% сярна киселина и вода (8) След кули 6 и 8 се монтират мокри електростатични утаители. 7 и 9. 75% сярна киселина, излизаща от дъното на измиващата кула 5, отива за отделяне на утайка, от която се изолират селен и арсен. Селенът отива в производството на полупроводници. 75% киселина, както и водни разтвори на сярна киселина, които се изхвърлят от колони 6 и 8 и електростатични утаители 7 и 9 отиват за производството на минерални торове. Електростатичните утаители 7 и 9. се използват за унищожаване на мъглата от сярна киселина. Така пречистеният газ от електростатичния утаител 9 навлиза в долната част на абсорбционната колона 10, където пещният газ се изсушава с помощта на 96-98% киселина. Търсената сярна киселина с концентрация 93-95% се отделя от дъното на колоната.
Пречистеният и изсушен газ от пещ през компресор 11 се подава през филтър 12 към топлообменна система (13 и 14) за нагряване до температура 400 градуса и се подава в контактна апаратура 15, състояща се от 5 катализаторни слоя. Първите 3 слоя се използват за първия етап на контакт, 4 и 5 за втория контактен етап. Началната концентрация на SO2 в пещния газ е 10%. Загряването на пещния газ в топлообменниците 13 и 14 се осъществява чрез контактен газ, който се взема след 1 и 3 слоя на катализатора. Степента на конверсия на SO2 в SO3 на първия слой на катализатора достига 70%, температурата на контактния газ се повишава до 600 градуса. Той преминава през тръбното пространство на топлообменника 14 и с температура 400 градуса навлиза в 2 катализаторния слой. След 2 слоя контактният газ се охлажда в топлообменника 18 и влиза в 3 катализаторния слой. След него контактният газ се охлажда в тръбното пространство на топлообменника 13 и се изпраща до първия етап на абсорбция, за да се възстанови полученият SO3. Поглъщането се извършва последователно в 2 абсорбатора 16 и 17. 16 абсорбаторът се напоява в горната част с 19% олеум, 20% олеум се отделя от дъното. Това е основният продукт на инсталацията. След това от 16 абсорбера контактният газ се изпраща в долната част на 17 абсорбатора, която се напоява с 98% сярна киселина. Отдолу 17 изхвърля приблизително 100% сярна киселина, която се използва за сушене. След извличане на SO3 от абсорбера 17 контактният газ се изпраща във втория етап на контакт в реактора 15 до каталитичния слой 4 и 5.
Контактният газ се нагрява в топлообменници от 20, 19, 18 до 400 градуса и влиза в 4 катализаторния слой. След него газът се охлажда в топлообменника 20 и влиза в петия слой на катализатора. След петия слой на катализатора, контактният газ се охлажда в топлообменника 19 и се подава до абсорбцията в абсорбера 21, който работи подобно на абсорбера 17.
Обратният газ със съдържание на серен оксид по-малко от 0,1% се отделя в атмосферата или се доставя за по-нататъшно пречистване в големи инсталации. Серните оксиди се превръщат или в смес от сулфити или сулфати или се редуцират до елементарна сяра.
Този метод на производство на сярна киселина ДК / ДА днес е технически модерен начин. Въпреки това има недостатъци.
На етапа на мокро почистване е необходимо да се охлажда и овлажнява, а за следващия етап е необходимо да се отцеди и загрее.
В момента е разработен нов метод за производство на сярна киселина - специална сярна киселина.
Полученият газ от пещта след почистване в сухи електростатични утаители се изпраща до контактна апаратура със специални катализатори, която не се страхува от контактни отрови и пари от влага. След това полученият контактен газ се изпраща за абсорбция с вода във фазата на парата. Веднага се научава сярна киселина под формата на мъгла, която се отлага върху мощни електростатични утаители. Има варианти на тази система, при която предварителният етап на катализация се използва за унищожаване на контактни отрови.
Обмислете процеса на получаване на сярна киселина по контактния метод от серни (железни) пирити. Първият етап на процеса е окисляването на пиритите с получаване на газ за изгаряне, съдържащ серен диоксид.
Изгарянето на пиритите (пирит) е сложен физичен и химичен процес и включва редица последователни или едновременно протичащи реакции:
Термична дисоциация 2FeS 2 \u003d 2FeS + S 2;
Парно-фазово изгаряне на сяра S 2 + 2O 2 \u003d 2SO 2;
Изгаряне на пиротит 4FeS + 7О 2 \u003d 2Fе 2 О 3 + 4SО 2.
Общата реакция: 4FеS 2 + 11O 2 \u003d 2Fе 2 О 3 + 8SO 2. (I)
С лек излишък или липса на кислород се образува смесен железен оксид:
3FеS 2 + 8O 2 \u003d Fe 3 О 4 + 6SO 2.
Термичното разлагане на пирита започва вече при температура около 200 ° С и сярата се запалва едновременно. При температура над 680 ° С и трите реакции протичат интензивно. В промишлеността стрелбата се извършва при 850 - 900 ° C. Ограничаващият етап на процеса е масовият пренос на продукти на разлагане в газовата фаза и окислителя към реакционното място. При същите температури твърдият компонент омеква, което допринася за адхезията на неговите частици.
Така в хода на реакцията (I), в допълнение към газообразния продукт на реакцията на SO2, се образува твърдият продукт Fe 2 O 3, който може да присъства в газовата фаза под формата на прах. Пиритът съдържа различни примеси, по-специално съединения от арсен и флуор, които по време на процеса на изпичане преминават в газова фаза. Наличието на тези съединения в етапа на контактно окисляване на серен диоксид може да причини отравяне с катализатор. Следователно, реакционният газ след етапа на изпичане на пирита трябва да бъде насочен предимно към етапа на подготовка за контактно окисляване (втори етап), който освен пречистване от каталитични отрови включва отделяне на водна пара (сушене), както и производството на странични продукти (Ce и Te).
На третия етап протича обратима екзотермична химическа реакция на контактно окисляване на серен диоксид:
SO 2 + 1 / 2O 2 ↔ SO 3
Различни метали, техните сплави и оксиди, някои соли, силикати и много други вещества имат способността да ускоряват окисляването на SO2. Всеки катализатор осигурява определена степен на преобразуване, характерна за него. При заводски условия е по-изгодно да се използват катализатори, с помощта на които се постига най-голяма степен на конверсия, тъй като остатъчното количество неокислен SO2 не се улавя в отделението за абсорбция, а се отстранява в атмосферата заедно с отработените газове.
Дълго време най-добрият катализатор за този процес се считаше за платина, която в ситно разделено състояние се прилага върху влакнести азбест, силикагел или магнезиев сулфат. Въпреки това, платината, въпреки че има най-висока каталитична активност, е много скъпа. В допълнение, неговата активност значително намалява при наличието на най-малки количества арсен, селен, хлор и други примеси в газа. Следователно използването на платинен катализатор доведе до усложнение на хардуерния дизайн поради необходимостта от цялостно пречистване на газа и повиши цената на крайния продукт.
Сред неплатиновите катализатори ванадийният катализатор (базиран на ванадиев пентоксид V 2 O 5) има най-висока каталитична активност, той е по-евтин и по-малко чувствителен към примеси от платиновия катализатор.
Окислителната реакция на SO2 е екзотермична; топлинният му ефект, като всяка химическа реакция, зависи от температурата. В диапазона 400-700 ° C топлинният ефект на окислителната реакция (в kJ / mol) може да се изчисли с точността, достатъчна за техническите изчисления по формулата
Q \u003d 10 142 -9.26T или 24 205 - 2.21T (в kcal / mol)
където T- температура, К.
Реакцията на окисляване на SO 2 до SO 3 е обратима. Константата на равновесие на тази реакция (в Pa -0.5) се описва от уравнението
където Pso 3, Pso 2, Po 2 са равновесните парциални налягания на SO 3, SO 2 и O 2, Pa.
стойност крзависи от температурата. Стойностите на K p в диапазона
390-650 ° С може да се изчисли по формулата
logK p \u003d 4905 / T - 7.1479
Степента на конверсия на SO 2, постигната в катализатора, зависи от неговата активност, състав на газ, продължителност на контакт на газ с катализатора, налягане и др. За газ от този състав теоретично възможно, тоест равновесната степен на конверсия зависи от температурата и се изразява с уравнението

При промишлени условия скоростта на окисление на SO 2 е от съществено значение. Скоростта на тази реакция зависи от количеството оксидиран серен диоксид за единица време на единица маса на катализатора и, следователно, консумацията на катализатор, размерите на контактния апарат и други технически и икономически показатели на процеса. Търси се процесът да води така, че скоростта на окисляване на SO 2, както и степента на преобразуване да са възможно най-високи.
Скоростта на окисляване на SO2 се характеризира с постоянна скорост

където к 0 коефициент; E- енергия на активиране, J / mol; R- универсална газова константа, 8,31 J / (mol-K); T- абсолютна температура, К.
От кинетичната теория на газовете е известно, че делът на молекулите, притежаващи енергия, достатъчна да осигури реакция при тяхното сблъскване, е до първо приближение д~ E / RT . По този начин, този термин в уравнението на скоростта на реакцията характеризира фракцията от ефективни сблъсъци, водещи до образуването на SO3 молекули. Експонент в израз д~ ElRT отрицателно; следователно, с повишаване на температурата, скоростта на реакцията се увеличава и с увеличаването Eнамалява.
Енергия за активиране Eреакцията на окисляване на SO2 до SO3 е много голяма, поради което без катализатор реакцията на хомогенното окисляване практически не се проявява дори при висока температура. В присъствието на твърди катализатори енергията на активиране намалява, следователно скоростта на хетерогенната каталитична реакция се увеличава. По този начин ролята на катализатора е да намали енергията на активиране E.
Последният етап от процеса е абсорбцията на серен триоксид с концентрирана сярна киселина или олеум.
Отделните етапи за получаване на сярна киселина могат да бъдат комбинирани по различни начини в технологичната схема на процеса. На фиг. 1 е схематична диаграма на процес за получаване на сярна киселина от пирити в съответствие с отворена верига с така наречения единичен контакт.
Най-важната задача при производството на сярна киселина е да се увеличи степента на превръщане на SO 2 в SO 3. В допълнение към увеличаване на производителността на сярна киселина, тази задача може да реши и екологични проблеми - да намали емисиите на вредния компонент SO 2 в околната среда,.
Увеличаването на степента на конверсия на SO 2 може да бъде постигнато по различни начини. Най-често срещаното от тях е създаването на схеми за двоен контакт и двойно поглъщане (DCDA).

Фиг. Функционална схема на производството на сярна киселина от пирити по метода на един контакт.
Друго възможно решение на същия проблем е да се проведе процесът в циклична (затворена) схема, използвайки технически кислород.
Трябва да се отбележи, че схемата, показана на фиг. 1 е само предварителна диаграма, която не съдържа голямо количество информация. Например, тя не отразява топлопреминаването между отделните потоци, което е необходимо за енергийно-технологичната схема, не посочва типовете устройства, използвани във всяка единица и пр. Възможно е да се решат тези проблеми, като се анализират физико-химичните и технологичните особености на отделните етапи на процеса.
От даденото на фиг. 1 схематична диаграма следва, че може да различи четири основни основни етапа:
1) получаване на калциниращ газ, съдържащ серен диоксид;
2) подготовка на газ за изгаряне за контактно окисляване;
3) каталитично окисляване на серен диоксид;
4) абсорбция на серен триоксид.
С различен технологичен дизайн някои детайли на тези етапи, особено етап 2, ще се различават, но принципният подход към тяхното изпълнение и изборът на технологичен режим зависи от задачите, които се решават на разглеждания етап, и ще бъдат еднакви в различни специфични процеси за производство на сярна киселина.

